La Trisomie 21 en quelques chiffres
Recherches autour de la trisomie 21
La trisomie21, par le Pr.Sarda

Qu’est-ce qui ne fonctionne pas chez le patient atteint de T 21 ?
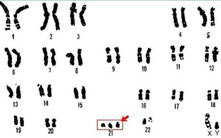
Les enfants qui ont une trisomie 21 ont un chromosome entier en plus donc ils ont des centaines et centaines de gènes en 3 exemplaires qui perturbent le fonctionnement cérébral dans tout un tas de fonctions. La conséquence est ce qu’on appelle une déficience intellectuelle, associée pour certains à des malformations; des malformations du cœur, malformations des reins… et avec un problème de croissance puisqu’on sait que ce sont des enfants qui seront plus petits que la moyenne des adultes.
La T21 est-elle une maladie évolutive ?
Non, pas du tout. Les anomalies chromosomiques comme la trisomie 21 ne sont pas des anomalies évolutives. On nait avec des difficultés. Les difficultés apparaissent avec l’âge. On ne nait pas en parlant mais on nait avec des difficultés dans la programmation des capacités du développement mais il n’y a pas de maladie évolutive tel qu’on peut le voir avec la maladie d’Alzheimer ou une pathologie qui va à un moment évoluer.
Comment est organisée la recherche en France, en Europe et sur la scène internationale ?
La recherche se fait à différents niveaux. Il y a ce qu’on appelle les recherches académiques qui sont les recherches des universités nationales. Comme c’est le cas en France pour la recherche qui est mise en place actuellement sur la trisomie 21. Il y a aussi des recherches qui peuvent être mises en place par un laboratoire pharmaceutique comme c’est le cas du laboratoire Hauffmann Laroche qui lance une recherche dans une déficience intellectuelle qui s’appelle le syndrome x fragile.
Les laboratoires vous sollicitent-ils ?
Les labos nous sollicitent. Ils ont un médicament à tester et ils nous sollicitent pour proposer éventuellement à nos patients que nous connaissons.
Pour la trisomie 21, c’est une recherche du même type qui est faite par les universités en particulier par la recherche nationale française – le ministère de la recherche.
Il y a donc une lien différencié entre le public et le privé ?
Oui, la concurrence est excellente de toute façon. Il vaut mieux être plusieurs que tout seul.
En France qui s’occupe de la recherche ?
Tous les ans, les hôpitaux ont des appels d’offres de projets de recherches. Au niveau académique, cela s’appelle des PHRC : protocole hospitalier de recherches cliniques. Il y a 2 ans, le CHU de Saint-Etienne a proposé une recherche dans la trisomie 21 à 6 centres du sud de la France pour une participation à cette recherche. On a tous les ans des appels à projets, des projets qui seront jugés. Si le projet est accepté, il sera accepté avec le financement.
Qui finance ?
Dans cet exemple, c’est l’Etat. Dans un projet académique, c’est l’Etat qui finance. Dans un projet privé, c’est le laboratoire privé qui finance.
Et la déontologie ?
Tous les projets passent devant des comités d’éthique. D’abord, au niveau des projets académiques, il y a une expertise. Peu de projets sont acceptés au bout du compte, 10 % seulement. Ce ne sont pas que des projets thérapeutiques. Les projets sont jugés non seulement sur leur importance scientifique, les débouchés qu’ils peuvent avoir mais aussi sur le côté éthique et le côté fondamental. Ensuite, les projets, lorsqu’ils sont acceptés sur le principe, doivent passer devant un comité d’éthique d’abord régional puis national.
Cela peut donc garantir l’impartialité des résultats face aux fonds privés ?
Même les fonds privés passent devant le comité éthique. Ils ont la même obligation. Tout le monde a la même obligation dans le cadre de recherches, surtout sur les recherches sur l’être humain. C’est plus que fondamental.
Si le chercheur valide la recherche demandée par le laboratoire, cela est tout bénéfique pour lui ?
Ce sera bénéfique. Mais maintenant faire une recherche pour un laboratoire privé pour une maladie rare, ce n’est pas quand même l’hypertension au diabète. C’est bien que des laboratoires privés se mettent dans cette recherche pour des maladies qui sont rares et qui n’intéressent pas financièrement beaucoup de laboratoires. Il faut en être convaincu.
Il y a donc un engagement certain derrière ?
C’est un engagement. C’est important. Il faut voir cela aussi à l’échelle mondiale. Même si une maladie est rare. A l’échelle mondiale, il y a plus des dizaines de milliers de personnes qui sont malades. Il y a un intérêt financier mais c’est des années et des années de recherches.

Combien de temps mettez-vous pour proposer un projet ?
Le projet sur la T21 qui doit débuter a d’abord fait l’objet de travaux très fondamentaux. Qu’est-ce que la T21 ? qu’est-ce qu’un chromosome supplémentaire ? Qu’est-ce qui vient bouleverser le fonction cérébral ? A priori c’est compliqué de le savoir.
On sait que sur le chromosome 21 il y a des gènes que l’on connait. On a commencé par réfléchir à l'utilité des centaines et centaines de gènes qui ont rôle dans la difficulté cérébrale. Ensuite on a pu créer des modèles de souris, on leur a mis un petit bout du chromosome 21 ou l’équivalent du chromosome de l’être humain. On a vu que ces souris avaient des difficultés de mémoire, de logiques, de développement. On a ensuite regardé comme s’exprimaient ces gènes dans le cerveau. On va regarder quels gènes ne modifient pas et ceux qui vont modifier le fonctionnement cérébral . Ensuite, on a vu que tels gènes perturbaient en excès. On a vu que tels médicaments pouvaient diminuer cet excès. Ce produit ou ce médicament peut avoir un intérêt si on diminue l’activité du gène dans le cerveau, cela a peut-être un intérêt ou pas. Il n’y a pas de modifications des difficultés. En particulier, on s’est aperçu sur un gène précis qui est en excès chez l’enfant trisomique, qu'une molécule particulière que l'on donnait à des souris améliorait leurs conditions. On s'est dit qu’à partir de ce moment là, si la souris est améliorée alors peut-être que l’être humain sera amélioré. Donc il faut que, cela représente des dizaines d’années, le produit existe. Qu’on vérifie qu’il n’y ai pas d’effets nocifs, que le produit n’est pas connu pour des effets secondaires. On va le donner à tester à des témoins sains adultes qui vont accepter de prendre cette molécule. On va vérifier qu’il n’y a aucun problème. Cela est vrai pour tous les médicaments. Si cet essai est concluant, on va trouver des personnes qui ont la maladie que l’on veut traiter par petit nombre. On va regarder que chez eux il n’y a pas d’effets nocifs secondaires. On n’est plus chez la personne saine. Si on contrôle qu’il n’y a pas d’effets secondaires embêtants chez le T21 adulte, il va falloir montrer qu’il est efficace. On va tirer au sort un groupe de trisomiques adultes volontaires qui va prendre le traitement et un groupe qui va prendre le placebo pendant une petite période. On va vérifier s’il y a un effet positif et le tester sur une plus grande période, tout en contrôlant qu’il n’y a pas d’effets négatifs. Ensuite, on va passer à des enfants au plus jeune âge. C’est des années et des années depuis la mise en place du concept jusqu’à ce qu’on prouve que cela est efficace. Le médicament sera accepté comme traitement après toutes ces vérifications.
Cela réduit les déficiences mais cela ne soigne pas ?
Cela ne guérit pas. On n'enlève pas un chromosome en plus. On le fera jamais à priori. On a des milliards de cellules. Nos milliards de cellules ont ce chromosome en plus. C’est impensable d’enlever un chromosome.
Pour les familles, quel espoir ces recherches représentent-elles ?
L’espoir, c’est d’améliorer la vie d’une personne trisomique ou x fragile ou d’une personne qui a une déficience intellectuelle ou atteinte d’une maladie génétique. On peut améliorer plusieurs difficultés. Dans l’x fragile, ce sont des patients qui sont extrêmement angoissés. Beaucoup sont considérés comme des autistes. Donc si on peut améliorer ce côté-là, la socialisation, le mieux être, l’angoisse, c’est déjà bien. Dans la trisomie 21, on va essayer d’améliorer leurs capacités intellectuelles.
Quand parle-t-on de déficience intellectuelle par rapport au Qi ?
On parle de déficience quand les personnes sont en-dessous des déviations standards soit en dessous de 70. Entre 70 à 130, on peut être considéré comme ayant un Qi normal avec une variabilité. Maintenant si vous avez un Qi à 80 mais d’énormes difficultés de langage, des difficultés psychologiques, cela vous rend la vie plus difficile ou l’acquisition des bases scolaires.
On parle alors de surhandicap ?
Oui, on peut parler de surhandicap. Le Qi ne veut pas tout dire. Vous pouvez avoir des problèmes de motricité fine ; énormément de mal à écrire. A l’école, vous allez être pénalisé même si votre Qi n’est pas si mauvais.
Le Qi donne quelque chose mais ensuite se surajoute tout un tas de capacités ou de déficiences. Par exemple, pour l’x fragile, son Qi est déficient mais il est surhandicapé par un comportement replié, autistique qui va entrainer une relation sociale très difficile. Si on peut améliorer ça, on va améliorer sa vie sans améliorer son Qi. A priori, ce n’est pas ce qui est pour l’instant recherché.
Dans vos recherches, la famille a donc un rôle important ?
Il faut que la famille participe. La famille de personne handicapées doit être d’accord ainsi que la personne elle-même. La famille doit avoir conscience qu’il ne faut pas attendre de bénéfice dès le lendemain. Le médicament sera validé qu’au bout de quelques années. Mais je pense qu’il y a une solidarité parmi ces familles et ces patients. Ceux qui ne peuvent pas avoir aujourd’hui et bien peut-être qu’un enfant dans 10 ans aura une vie complètement bouleversée grâce à ce que cette famille aura apporté. C’est important et gratifiant pour une famille d’être là pour faire avancer. Ces maladies rares sont basées sur la solidarité de génération en génération. C’est important car sans les familles, on ne peut pas faire de recherches. Et on ne pourra pas dans 5 ans, dans 10 ans mieux aider les gens.
Comment une personne T21 peut participer, par exemple, à un essai clinique ?
Il y a une consultation trisomique 21 d'enfants et d'adultes puisqu’en génétique on suit les patients quelque soit leur âge. On le propose à des patients connus. De plus, au travers du réseau « Vivre avec une anomalie en Languedoc Roussillon », on a passé l’information. Vous êtes là aujourd’hui. Mon rôle est de faire passer l’information à ceux qui veulent la connaître. Maintenant, c’est aux personnes de décider si elles veulent participer ou pas. Je m’appuie sur les médias. Je pense que mon rôle est de dire aux familles qu’il y a des choses qui se mettent en place et si cela les intéresse, elles peuvent venir nous voir pour qu'on leur expliquer.
Pourquoi avez-vous créé le Réseau Maladies Rares Méditerranée?
Il a été réfléchi en fin 2007 puis la création effective en 2008. En général, c’est très difficile de trouver des professionnels pour aider les personnes atteintes d'une maladie rare avec une anomalie du développement. Ce sont des enfants qui ont des handicaps multiples. Par exemple, un enfant qui a des difficultés dans son développement doit faire de la kiné, de la psychomotricité, de l’orthophonie, de l’ergothérapie… Il est intégré au niveau scolaire dans des classes particulières. C’est difficile quand on n’habite pas Montpellier de trouver des professionnels qui aident ces familles et ces patients.
Surtout au niveau de l’annonce du handicap, les professionnels ont des efforts à faire car le ressenti des parents est très violent.
La santé n’a pas de prix ?
Oui, elle a un coût. Mais il faut voir à l’échelle mondiale. On n’a pas de frontière. On est dans des maladies rares. Il y a peu de gens qui investissent. Il faut que les laboratoires s’y retrouvent sinon les laboratoires ne font pas de recherches et les patients n’ont pas de médicaments.
Professeur Pierre Sarda
Département de Génétique Médicale, Maladies Rares et Médecine Personnalisée
CHU de Montpellier - Hôpital Arnaud de Villeneuve
https://www.maladiesraresinfo.org/
Recherche : In vitro...
In vitro, des chercheurs réduisent la trisomie 21 au silence.
Généralement empreints de sécheresse et de rigueur, les titres des articles scientifiques ne rendent souvent pas justice à la profondeur des expériences qu'ils décrivent ni à l'ingéniosité des chercheurs qui les ont effectuées. C'est le cas d'une étude publiée ce mercredi 17 juillet dans la revue Nature. Son titre, "Translating dosage compensation to trisomy 21", masque bien le petit exploit qu'a réalisé l'équipe américano-canadienne qui en est l'auteur : réduire, in vitro, la trisomie 21 au silence. Autrefois connue sous le nom affreux de "mongolisme", la trisomie 21 est une anomalie chromosomique : au lieu de se trouver en deux exemplaires dans les cellules, le chromosome 21 y est présent trois fois (d'où le nom de trisomie). Ce chromosome surnuméraire crée une surdose de gènes et des molécules dont ces derniers commandent la production, surdose qui entraîne, chez les personnes porteuses de la trisomie, un certain nombre d'anomalies physiques et, surtout, un retard cognitif.
Dans cette étude de Nature, les chercheurs sont parvenus non pas à retirer ce chromosome de trop mais à l'inactiver. Et pour ce faire, ils se sont simplement servis d'un mécanisme naturel à l'œuvre chez la moitié des êtres humains peuplant cette Terre, les femmes. Le sexe de chacun d'entre nous est déterminé par une paire de chromosomes dits sexuels, XY chez ces messieurs, XX chez ces dames. Mais le chromosome X ne sert pas qu'à "dire" le sexe : il porte de nombreux autres gènes. Or, on s'aperçoit, en regardant l'exemple masculin, qu'une seule copie de ce chromosome suffit. Le "problème" des femmes, c'est qu'elles en portent deux, ce qui est donc un de trop. Pour empêcher que, comme dans le cas de la trisomie 21, ce chromosome surnuméraire ne provoque une surdose, un des deux membres de la paire est donc mis entre parenthèses. Très tôt dans le développement de l'embryon féminin, un des deux chromosomes produit, via un gène nommé Xist, une grande quantité d'ARN non codant qui va littéralement enrober le chromosome et le recroqueviller, un peu comme une araignée entoure sa proie d'un cocon de soie. Le chromosome X inactivé se retrouve à terme sur une voie de garage, collé à la paroi du noyau cellulaire, sous la forme de ce que les biologistes appellent un corpuscule de Barr.
Pour leur expérience, les chercheurs ont tout d'abord prélevé des cellules d'un patient trisomique et les ont reprogrammées en cellules souches, afin de pouvoir ensuite les différencier à leur guise en tout type de cellules. Puis ils ont effectué une sorte de "copier-coller" en prenant le gène Xist et en l'insérant dans un des trois chromosomes 21. En l'espace de quelques jours, ce gène a fait son travail et emmailloté ce chromosome surnuméraire. Ce dernier a fini sur la touche, transformé en corpuscule de Barr. Les auteurs de l'étude ont ensuite procédé à plusieurs examens pour vérifier l'efficacité du processus. Ils se sont notamment intéressés à deux gènes portés par le chromosome 21 : le gène de l'enzyme DYRK1A dont la surexpression semble liée à l'apparition du retard mental chez les trisomiques et le gène de la protéine APP qui, surproduite, explique le risque accru qu'ont les personnes atteintes de trisomie 21 de développer la maladie d'Alzheimer. Dans les deux cas, les gènes ont été pour tout ou partie réprimés.
L'expérience est élégante mais, ainsi que me l'a expliqué Jean-Maurice Delabar, directeur de recherches au CNRS et responsable d'une équipe à l'unité de Biologie fonctionnelle et adaptative (université Paris-Diderot) qui travaille sur la trisomie 21, "il ne faut pas s'imaginer qu'on va demain, comme par enchantement, inactiver le chromosome supplémentaire chez les personnes atteintes de trisomie 21". Il souligne que, tout comme pour le second chromosome X des femmes, dont l'inactivation n'est jamais totale, le procédé n'est pas complètement efficace. Au niveau de la cellule, en passant de trois à deux chromosomes actifs, on pourrait s'attendre à une réduction d'expression des gènes d'un tiers. Or, comme le fait remarquer M. Delabar, "dans l'étude, cette réduction est plutôt de l'ordre de 20 %". Le chercheur français veut surtout retenir dans cette étude l'outil qu'elle fournit pour examiner les chemins qu'emprunte la trisomie pour dérégler le bon fonctionnement des cellules et de l'organisme.
Les auteurs de l'article sont d'ailleurs sur la même longueur d'onde et restent prudents quand ils évoquent une application thérapeutique de leur technique. A ma demande, Jean-Maurice Delabar s'est tout de même projeté dans l'hypothèse où cette stratégie d'inactivation chromosomique serait viable : "Le principal problème dans la trisomie 21 étant cognitif, m'a-t-il expliqué, on peut imaginer de cibler les populations neuronales. On sait depuis plusieurs années que le cerveau produit en continu des neurones au cours de la vie : on pourrait faire en sorte de remplacer un certain nombre de neurones surexprimant des protéines par des neurones qui en expriment une quantité normale. Une petite fraction peut éventuellement suffire à provoquer des améliorations. On est dans la science-fiction mais c'est une possibilité future." Si cela se concrétise, on se souviendra probablement de cet article de 2013 comme de celui qui, après la thérapie génique, a ouvert la voie à la thérapie chromosomique.

